荔园非编码RNA平台——miRNA的qPCR检测
实验原理
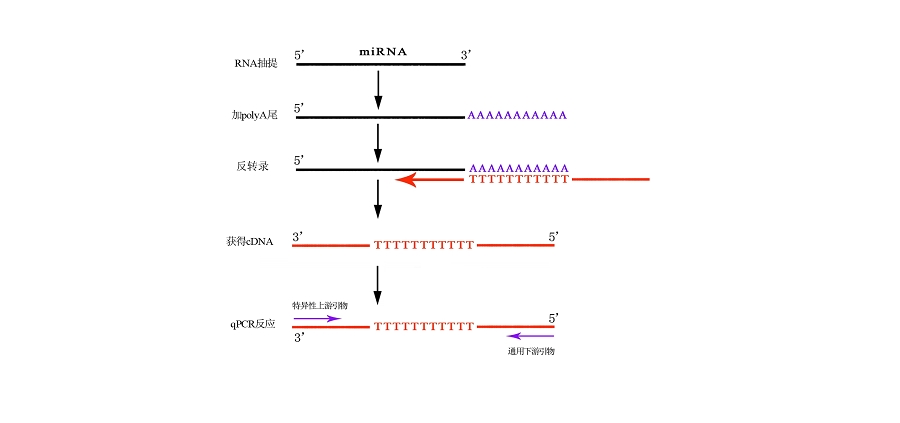
通过qPCR准确进行miRNA在细胞或组织样本中的表达分析是研究miRNA功能的基础。将小片段的miRNA通过聚合酶A加尾,再通过含有通用序列的Oligo序列进行反转录,合成特异性的miRNA引物及通用引物即可对miRNA进行qPCR检测工作。(见下图)
![]()
图1 miRNA的qPCR检测原理示意图
技术应用
研究miRNA与疾病的相关性,开发miRNA作为疾病诊断及治疗生物标志物。
实验流程
![]()
![]()
实验结果实例
![]()
图1 目的基因hsa-miR-9-1 在不同样本中的qPCR相对定量检测结果的
1)目的基因hsa-miR-9-1 的扩增曲线和熔解曲线;2)内参基因人 snRNA U6的扩增曲线和熔解曲线;
3)hsa-miR-9-1 在不同样本中的qPCR相对定量检测柱形图。
TROUBLESHOOTING
|
实验问题
|
原因
|
推荐解决方法
|
|
溶解曲线出现杂峰?
|
RNA被基因组DNA污染
|
用DNase处理样本。
|
|
引物二聚体
|
降低引物使用浓度。
|
|
非特异性扩增
|
冰上配置,降低模板量,提高退火温度。
|
|
扩增产物量少?
|
靶miRNA基因表达量低或者无表达
|
增加高表达miRNA的阳性对照样本以验证反应体系。
|
|
模板量低
|
提高模板量或增加循环数。
|
|
扩增曲线不正常?
|
反应体系中存在酶抑制导致PCR酶失活
|
重新抽提RNA,注意反应体系匆引入酶抑制剂。
|
|
染料降解
|
更换荧光定量PCR反应体系。
|
|
模板质量问题
|
提高模板的纯度。
|
常见问题 FAQ
Q :如何选择miRNA荧光定量PCR的阳性对照样本?
A :请参考相关文献确认高表达miRNA的细胞作为阳性对照细胞,以验证特异性引物的设计没有问题。
Q :miRNA荧光定量PCR选用何种基因作为内参基因?
A :起始样本量、PNA制备和定量、反转录效率的差异都可能导致荧光定量PCR的误差,内源性对照基因是纠正初始样本量,反转录效率的最准确的方法。
Small nuclear RNA (snRNA)和small nucleolar RNA (snoRNA)长度与miRNA相近,200bp左右,在多种组织、细胞中高表达,不涉及miRNA的调节途径,且引物设计方法相同,都是很好的内参选择,如最为常用的miRNA内参基因为snRNA U6。
Q :提供的miRNA的qPCR引物设计有何特点?
A :由于miRNA本身片段短,设计有局限性,因此miRNA的qPCR引物设计要求比普通qPCR要求,我们可以为您设计合成特异性更高、扩增效率更高的引物,并且各个引物Tm值均一、扩增片段性质均一,所有引物可采用同一反应条件进行扩增。
参考文献
1.Suzuki T, Higgins PJ, Crawford DR. Control selection for R N A quantitation. Biotechniques 2000,29(2):332-337.

 微信扫码
微信扫码
 热线电话
热线电话
 用户中心
用户中心
 意见反馈
意见反馈

 荔园基因
荔园基因

 购物车
购物车